Chapitre 3 : Les ions
I) Qu'est ce qu'un ion?
Un ion est un atome ou un groupement d’atomes qui a perdu ou gagné un ou plusieurs électrons.
Il existe des ions positifs qui ont perdu des électrons et des ions négatifs qui en ont gagné.
Exemple formation de l'ion Sodium :
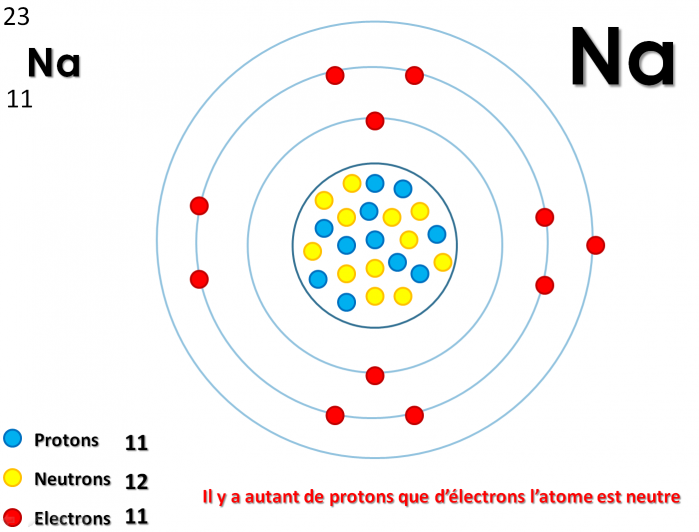
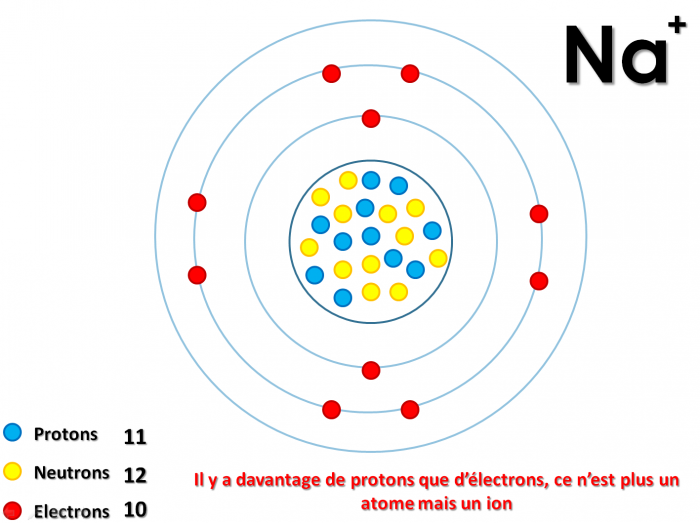
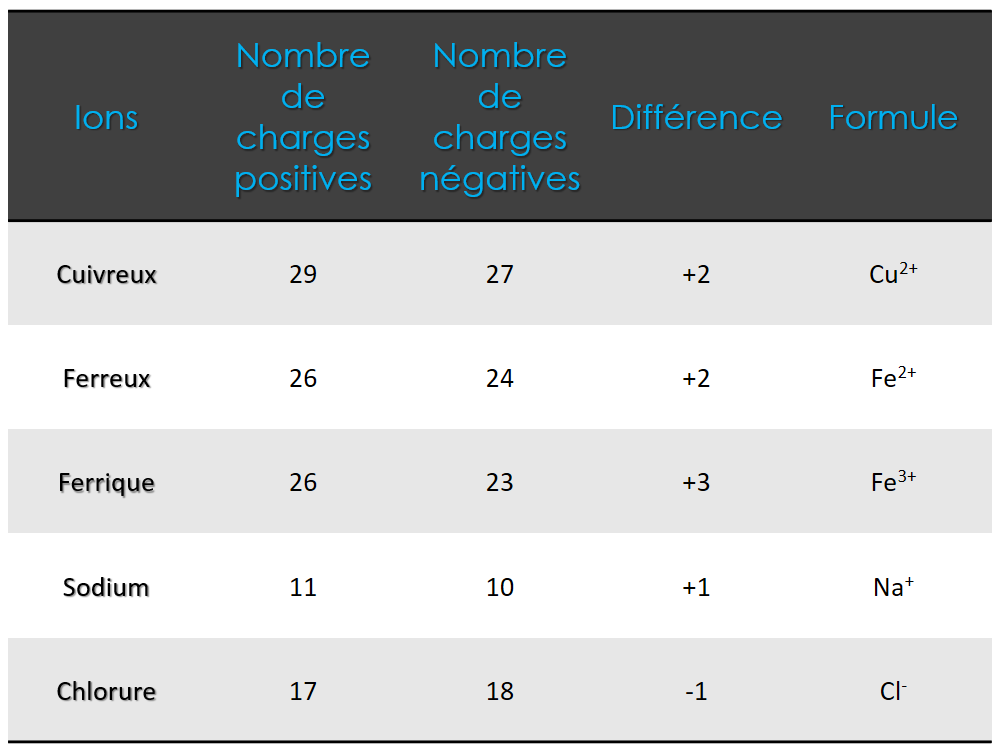
II) Test des ions
- On introduit dans un tube à essai quelques mL de solution contenant des ions que l'on cherche à identifier.
- Dans ce Tube on introduit quelques gouttes de réactif testeur.
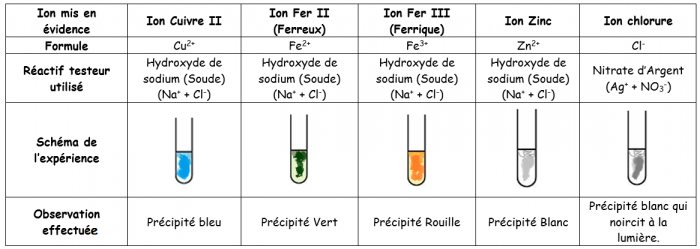
==> Test de reconnaissance des ions Cuivre (Cu2+) : Réactif utilisé la Soude (Hydroxyde de sodium)
En présence de soude, les ions Cu2+ forment un précipité bleu.
==> Test de reconnaissance des ions Zinc (Zn2+): Réactif utilisé la Soude (Hydroxyde de sodium)
En présence de soude, les ions Zn2+ forment un précipité blanc. Si on met beaucoup de soude, ce précipité se dissout et la solution redevient incolore
==> Test de reconnaissance des ions Fer II (Fe2+): Réactif utilisé la Soude (Hydroxyde de sodium)
En présence de soude, les ions Fe2+ forment un précipité vert.
==> Test de reconnaissance des ions Fer III (Fe3+): Réactif utilisé la Soude (Hydroxyde de sodium)
En présence de soude, les ions Fe3+ forment un précipité rouille.
==> Test de reconnaissance des ions Chlorure Cl-: Réactif utilisé le Nitrate d’argent.
En présence de nitrate d’argent, les ions Cl- forment un précipité blanc qui noircit à la lumière.

Voir la fiche méthode : Comment identifier un ion








